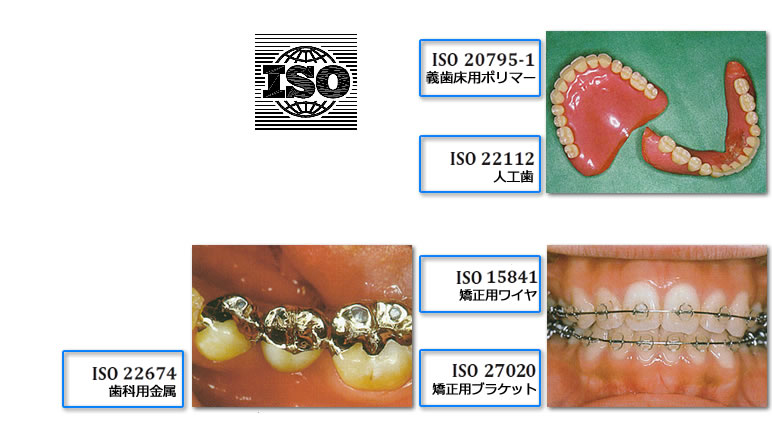
ISOといえば、一般にはISO 9001などの認証規格が知られています。
例えば、歯科医院でISO 9001の認証を取得すれば、デンタルヘルスサービスの質を保証する業務と管理の仕組みを、国際規格に合わせて実施していると認められます。
この認証規格とは別に、歯科に関する重要なISO規格があります。
何が、どう大切なのか。
歯科関連のISO規格について、日本歯科材料器械研究協議会の山本桂子事務局長にお話を伺いました。
■JISとISO規格の関係
ISO規格とは、ISO(International Organization Standardization:国際標準化機構)が発行した国際規格です。
ISOは、各国の代表的な標準化機関によって組織される非政府国際機関で、電気・電子分野及び電気通信分野を除くすべての産業分野について、国際的な標準化を行っています。
日本からは、JISを制定する日本工業標準調査会(JISC)が代表機関として参加しています。
ISO規格は、製品やサービスが安全で信頼性が高く、良質であることを確保するための要件を提供します。
各国が自国の国家規格を制定する際に、その分野に該当するISO規格が存在する場合は、WTO(世界貿易機関)/TBT協定(国際貿易を円滑にすることを目的とした、国際貿易の技術的障壁をなくすための協定)によって、ISO規格を基礎とすることが義務付けられています。
■安心と安全の証
そもそもなぜ、ISO規格やJISのような規格が必要なのでしょうか。
もし、トイレットペーパーに関するJISが存在しないとどうなるのでしょう。
各メーカーが自社の都合に合わせて製品を生産すれば、サイズや品質がまったく異なるトイレットペーパーが店頭に並びます。
その結果、自宅のトイレの紙巻器に収まらない商品を買ってしまったり、買った商品の品質が悪いため水に溶けず便器が詰まるおそれがあります。
こうした問題を防ぐために、トイレットペーパーに関するJISには、「紙幅」や水に触れたときの「ほぐれやすさ」などが定められています。
だから、JISに適合した製品ならば、誰もが安心して使えるのです。
ISO規格は、これを世界レベルに拡張したものです。
つまり、ISO規格に適合していれば、世界のどこでも品質が一定以上で、互換性があり、医療分野においても、安心して使えるということになるのです。
歯科医の先生方に注意していただきたいのは、海外から個人輸入された製品の使用です。
歯科医は自ら使用する医療機器の個人輸入が認められています。
本来、国内で市販されている海外の医療機器は、製造販売業者が医薬品医療機器等法による製造販売承認・認証・届出等の手続きを行った上で輸入するものに限られますが、個人輸入した製品の品質は保証されておらず、患者さんにその説明を行った上で使用しなければなりません。
■医薬品医療機器等法とISO規格
JISやISO規格自体はあくまでも任意規格であり、強制力は持ちません。
ただし、医薬品医療機器等法などの国家の規制の承認、認証等の基準として引用されることにより、その有用性が発揮されることになります。
日本では2005年に薬事法(現在の医薬品医療機器等法)の大幅な改正が実施され、医療機器の製造販売認証基準にJISが引用されることになり、製造販売承認基準にISO規格が引用されることになりました。
ここで重要となるのは、ISO規格とJISの関係です。
前述のWTO/TBT協定によって、対応するISO規格がある場合には、JISなどの国家規格はそれと整合させることが義務付けられているため、ISO規格で規定される内容が、日本(メーカー、歯科医及び患者)に不利益を被らないようにすることが大切です。
もし、ISO規格とJISが整合していなければ、JISに適合していない海外製品の輸入や、ISO規格に適合していない日本製品の輸出が困難となってしまいます。
ISO規格の開発は、ISOの各専門委員会によって行われていまして、歯科に関するISO規格は、ISO/TC 106(歯科専門委員会)で開発されています。
国内においては、経済産業省からISO/TC 106の業務を委託された日本歯科材料器械研究協議会が、歯科製造企業(生産者)、日本歯科医師会(使用者)、大学研究機関(中立者、使用者)の代表者で構成する国内委員会を設置し、臨産学の協働体制で対応しています。
歯科関連のISO規格は現在180件あり、改正作業を含む開発中のプロジェクトは51件(2018年6月1日現在)、ここ数年の年間規格発行件数は平均15件です。
■国内調整を尽くし国際会議に臨む
 国内委員会での検討段階でも、立場による意見の相違があります。
メーカーとしては、安全性は優先するとしても、試験方法を簡素化するなど可能な限りコストを抑えたいと考えます。
これに対して歯科医や患者サイドからすれば、安全性の確保が最優先と考えます。
その調整を図る私たちのスタンスは、製造業者と使用者に加えて、アカデミアの中立的及び学術的な見地からの意見を考慮して、日本の意見をまとめ、投票時に技術的な変更を要求するコメントを提出したり、国際会議の場で主張して、出来る限り、ISO規格をそのままJISにできるようにすることです。
例えば、日本人と欧米人とでは、体格や手の大きさ、眼球の色が異なります。
麻酔薬の量、器具の長さ、照明器具の適切な照度も違って当然であり、日本人に適切な量、サイズ、照度も規格に採用する必要が出てきます。
このようなことに対応するには、国際会議に積極的に参加し、日本の意見を強く主張していかなければなりません。
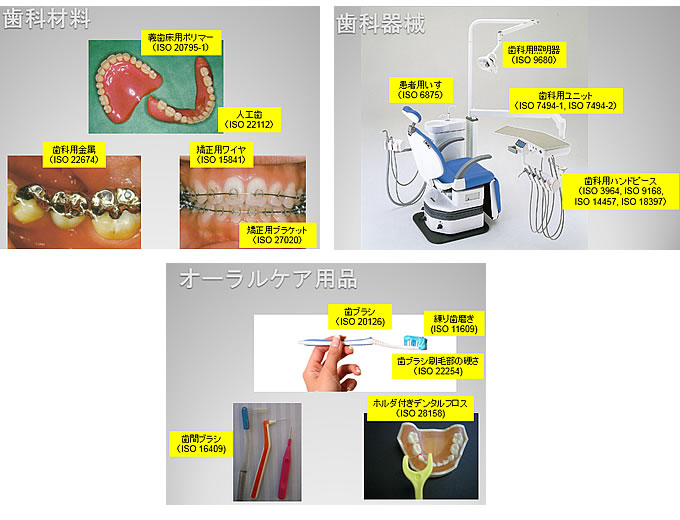
ISO/TC 106の傘下には、SC 1(充填修復材)、SC 2(補綴材料)、SC 3(用語)、SC 4(歯科器具)、SC 6(歯科器械)、SC 7(オーラルケア用品)、SC 8(歯科用インプラント)及びSC 9(歯科用CAD/CAMシステム)の8つのSC(Sub-committee)が設置されています。
具体的な規格開発作業は、各SC傘下にあるワーキンググループで進められるため、ここでの議論に参加して日本の意見を主張します。
ISOは一国一票制度で投票が行われるため、参加国の多いヨーロッパが優位です。
各ワーキンググループの参加国がだいたい15~20カ国として、平均すると半分以上の票がヨーロッパ諸国によって占められており、アジア圏は日本、中国、韓国及びタイの4か国だけです。
こうした状況において、日本の意見を通していくためには、アジア諸国はもちろん、アメリカやオーストラリアなどの英語圏のエキスパートとの連携が必要となります。
国内委員会での検討段階でも、立場による意見の相違があります。
メーカーとしては、安全性は優先するとしても、試験方法を簡素化するなど可能な限りコストを抑えたいと考えます。
これに対して歯科医や患者サイドからすれば、安全性の確保が最優先と考えます。
その調整を図る私たちのスタンスは、製造業者と使用者に加えて、アカデミアの中立的及び学術的な見地からの意見を考慮して、日本の意見をまとめ、投票時に技術的な変更を要求するコメントを提出したり、国際会議の場で主張して、出来る限り、ISO規格をそのままJISにできるようにすることです。
例えば、日本人と欧米人とでは、体格や手の大きさ、眼球の色が異なります。
麻酔薬の量、器具の長さ、照明器具の適切な照度も違って当然であり、日本人に適切な量、サイズ、照度も規格に採用する必要が出てきます。
このようなことに対応するには、国際会議に積極的に参加し、日本の意見を強く主張していかなければなりません。
ISO/TC 106の傘下には、SC 1(充填修復材)、SC 2(補綴材料)、SC 3(用語)、SC 4(歯科器具)、SC 6(歯科器械)、SC 7(オーラルケア用品)、SC 8(歯科用インプラント)及びSC 9(歯科用CAD/CAMシステム)の8つのSC(Sub-committee)が設置されています。
具体的な規格開発作業は、各SC傘下にあるワーキンググループで進められるため、ここでの議論に参加して日本の意見を主張します。
ISOは一国一票制度で投票が行われるため、参加国の多いヨーロッパが優位です。
各ワーキンググループの参加国がだいたい15~20カ国として、平均すると半分以上の票がヨーロッパ諸国によって占められており、アジア圏は日本、中国、韓国及びタイの4か国だけです。
こうした状況において、日本の意見を通していくためには、アジア諸国はもちろん、アメリカやオーストラリアなどの英語圏のエキスパートとの連携が必要となります。
■求められる現場の声
 国際会議は年に1回、約20か国から300名ぐらいが参加して、3日間の日程で各ワーキンググループの会議があり、その翌日にSC総会、最終日にTC 106の全体総会が開催されます。
これらすべてに参加しているのは日本、アメリカとドイツぐらいです。
日本からの出席者は、日本歯科医師会の器材・薬剤担当の常務理事の先生を団長として、日本歯科医師会及び日本歯科医学会から派遣された大学の先生やメーカー関係者で構成され、2017年の香港会議には90名程度が参加しました。
ISO規格開発は、年間を通じて随時、新たな規格案(又は、既存規格の改正)が提案され、その規格が現在の市場で必要かどうかが、各国の投票にかけられます。
承認条件が満たされれば、新業務項目として登録され、規格原案の検討がスタートします。
新規登録から発行にいたるまでには約3年の時間をかけて、原則的に3回の投票が行われます。
重要なのは第1回目の投票であり、関連するJISがある場合は、そのJISとの整合を図るために、技術的な変更を要求します。
前述したように、日本の意見は、メーカーだけでなく、歯科医及びアカデミアの意見も尊重しています。
医療現場で実際に医療機器を使用する歯科医の意見は、安全性や操作性を重視することからも大変重要です。
実際に、国際会議の場では、アメリカ、フランス、タイ、カナダなどは、歯科医師会からの代表委員が活躍しています。
日本歯科医師会は、器械規格委員会及び材料規格委員会を設置してJIS原案について検討していて、委員には一般開業医の先生にもご参画いただいています。
日常使用している医療機器が、日本の歯科医にとって、安心して使うことができる、操作性の良い製品、ひいては患者にとっても安心して治療を受けられるようになるために、歯科医の先生方にも、ISO規格の開発には使用者としての歯科医の意見も大切であり、それを規格に反映させることができることをご理解いただき、歯科材料、歯科器具や歯科器械だけでなく、オーラルケア用品に対する使用者の意見を聞かせていただきたいと思います。
国際会議は年に1回、約20か国から300名ぐらいが参加して、3日間の日程で各ワーキンググループの会議があり、その翌日にSC総会、最終日にTC 106の全体総会が開催されます。
これらすべてに参加しているのは日本、アメリカとドイツぐらいです。
日本からの出席者は、日本歯科医師会の器材・薬剤担当の常務理事の先生を団長として、日本歯科医師会及び日本歯科医学会から派遣された大学の先生やメーカー関係者で構成され、2017年の香港会議には90名程度が参加しました。
ISO規格開発は、年間を通じて随時、新たな規格案(又は、既存規格の改正)が提案され、その規格が現在の市場で必要かどうかが、各国の投票にかけられます。
承認条件が満たされれば、新業務項目として登録され、規格原案の検討がスタートします。
新規登録から発行にいたるまでには約3年の時間をかけて、原則的に3回の投票が行われます。
重要なのは第1回目の投票であり、関連するJISがある場合は、そのJISとの整合を図るために、技術的な変更を要求します。
前述したように、日本の意見は、メーカーだけでなく、歯科医及びアカデミアの意見も尊重しています。
医療現場で実際に医療機器を使用する歯科医の意見は、安全性や操作性を重視することからも大変重要です。
実際に、国際会議の場では、アメリカ、フランス、タイ、カナダなどは、歯科医師会からの代表委員が活躍しています。
日本歯科医師会は、器械規格委員会及び材料規格委員会を設置してJIS原案について検討していて、委員には一般開業医の先生にもご参画いただいています。
日常使用している医療機器が、日本の歯科医にとって、安心して使うことができる、操作性の良い製品、ひいては患者にとっても安心して治療を受けられるようになるために、歯科医の先生方にも、ISO規格の開発には使用者としての歯科医の意見も大切であり、それを規格に反映させることができることをご理解いただき、歯科材料、歯科器具や歯科器械だけでなく、オーラルケア用品に対する使用者の意見を聞かせていただきたいと思います。
日本歯科材料器械研究協議会
ISO/TC 106(国際標準化機構/歯科専門委員会)に関する国内審議団体として、1977年に設立。
日本はISO/TC 106年次会議に1977年から公式参加しており、1980年にP-メンバー(投票及び会議参加の義務を持つ会員)になっている。
その主要業務は、JISC(ISO会員団体、Japanese Industrial Standards Committee)のTC 106に関する業務を行い、歯科器材の国際標準化に貢献するとともに、JIS(日本工業規格、Japanese Industrial Standards)との整合化を図り、歯科器材の合理化、発展に寄与することである。

国内委員会での検討段階でも、立場による意見の相違があります。 メーカーとしては、安全性は優先するとしても、試験方法を簡素化するなど可能な限りコストを抑えたいと考えます。 これに対して歯科医や患者サイドからすれば、安全性の確保が最優先と考えます。 その調整を図る私たちのスタンスは、製造業者と使用者に加えて、アカデミアの中立的及び学術的な見地からの意見を考慮して、日本の意見をまとめ、投票時に技術的な変更を要求するコメントを提出したり、国際会議の場で主張して、出来る限り、ISO規格をそのままJISにできるようにすることです。 例えば、日本人と欧米人とでは、体格や手の大きさ、眼球の色が異なります。 麻酔薬の量、器具の長さ、照明器具の適切な照度も違って当然であり、日本人に適切な量、サイズ、照度も規格に採用する必要が出てきます。 このようなことに対応するには、国際会議に積極的に参加し、日本の意見を強く主張していかなければなりません。 ISO/TC 106の傘下には、SC 1(充填修復材)、SC 2(補綴材料)、SC 3(用語)、SC 4(歯科器具)、SC 6(歯科器械)、SC 7(オーラルケア用品)、SC 8(歯科用インプラント)及びSC 9(歯科用CAD/CAMシステム)の8つのSC(Sub-committee)が設置されています。 具体的な規格開発作業は、各SC傘下にあるワーキンググループで進められるため、ここでの議論に参加して日本の意見を主張します。 ISOは一国一票制度で投票が行われるため、参加国の多いヨーロッパが優位です。 各ワーキンググループの参加国がだいたい15~20カ国として、平均すると半分以上の票がヨーロッパ諸国によって占められており、アジア圏は日本、中国、韓国及びタイの4か国だけです。 こうした状況において、日本の意見を通していくためには、アジア諸国はもちろん、アメリカやオーストラリアなどの英語圏のエキスパートとの連携が必要となります。
国際会議は年に1回、約20か国から300名ぐらいが参加して、3日間の日程で各ワーキンググループの会議があり、その翌日にSC総会、最終日にTC 106の全体総会が開催されます。 これらすべてに参加しているのは日本、アメリカとドイツぐらいです。 日本からの出席者は、日本歯科医師会の器材・薬剤担当の常務理事の先生を団長として、日本歯科医師会及び日本歯科医学会から派遣された大学の先生やメーカー関係者で構成され、2017年の香港会議には90名程度が参加しました。 ISO規格開発は、年間を通じて随時、新たな規格案(又は、既存規格の改正)が提案され、その規格が現在の市場で必要かどうかが、各国の投票にかけられます。 承認条件が満たされれば、新業務項目として登録され、規格原案の検討がスタートします。 新規登録から発行にいたるまでには約3年の時間をかけて、原則的に3回の投票が行われます。 重要なのは第1回目の投票であり、関連するJISがある場合は、そのJISとの整合を図るために、技術的な変更を要求します。 前述したように、日本の意見は、メーカーだけでなく、歯科医及びアカデミアの意見も尊重しています。 医療現場で実際に医療機器を使用する歯科医の意見は、安全性や操作性を重視することからも大変重要です。 実際に、国際会議の場では、アメリカ、フランス、タイ、カナダなどは、歯科医師会からの代表委員が活躍しています。 日本歯科医師会は、器械規格委員会及び材料規格委員会を設置してJIS原案について検討していて、委員には一般開業医の先生にもご参画いただいています。 日常使用している医療機器が、日本の歯科医にとって、安心して使うことができる、操作性の良い製品、ひいては患者にとっても安心して治療を受けられるようになるために、歯科医の先生方にも、ISO規格の開発には使用者としての歯科医の意見も大切であり、それを規格に反映させることができることをご理解いただき、歯科材料、歯科器具や歯科器械だけでなく、オーラルケア用品に対する使用者の意見を聞かせていただきたいと思います。